Chiều 3/2, Cục Quản lý Dược (Bộ Y tế) đã có thông tin về sinh phẩm Evusheld. Theo đơn vị này, Evusheld là sinh phẩm kết hợp bộ đôi kháng thể đơn dòng (tixagevimab 150mg/1,5ml và cilgavimab 150mg/1,5ml) được AstraZeneca phát triển với chỉ định dự phòng trước phơi nhiễm Covid-19 ở người lớn và thanh thiếu niên từ 12 tuổi trở lên có trọng lượng ít nhất 40kg.
Evusheld đã được cấp phép lưu hành bởi nhiều cơ quan quản lý, bao gồm các hình thức cấp phép lưu hành có điều kiện, cấp phép sử dụng khẩn cấp và các hình thức khác nhằm hỗ trợ tiếp cận sớm với thuốc (Early access) và hiện Evusheld đã được sử dụng tại gần 40 quốc gia trên thế giới với chỉ định điều trị và/hoặc dự phòng phơi nhiễm Covid-19.
Tại Việt Nam, Cục Quản lý Dược cho biết thuốc Evusheld đã được cấp giấy đăng ký lưu hành ngày 25/10/2022.
Ngày 26/1/2023, Cơ quan quản lý thực phẩm và dược phẩm Hoa Kỳ (USFDA) có thông báo tạm dừng cấp phép sử dụng trong trường hợp khẩn cấp thuốc Evusheld cho tới khi có thông báo cập nhật của USFDA với lý do Evusheld không có tác dụng bảo vệ đối với một số biến chủng mới của SARS-CoV-2 hiện đang chiếm ưu thế tại Hoa Kỳ, như biến chủng phụ XBB.1.5 của Omicron (hiện có hơn 90% ca nhiễm do biến chủng này tại Hoa Kỳ).
Theo USFDA, việc sử dụng Evusheld sẽ bị giới hạn cho đến khi tỉ lệ biến chủng SARS-CoV-2 không nhạy cảm với Evusheld ở Hoa Kỳ giảm xuống dưới 90%.
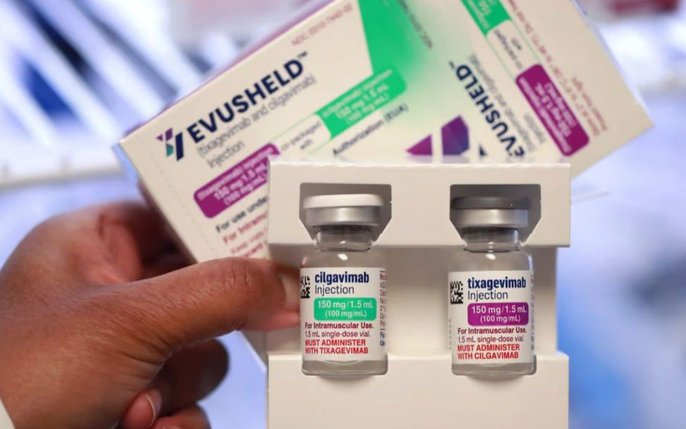
Ngày 26/1/2023, USFDA thông báo tạm dừng cấp phép sử dụng trong trường hợp khẩn cấp thuốc Evusheld.
Ngoài ra, USFDA khuyến cáo các cơ sở y tế và nhà cung cấp Evusheld vẫn nên giữ lại các chế phẩm hiện có để bảo quản theo quy định và sử dụng trong trường hợp các biến chủng của SARS-CoV-2 mà Evusheld chống lại được trở nên phổ biến hơn ở Hoa Kỳ.
Cho đến thời điểm ngày 30/1/2023, Evusheld vẫn được cho phép lưu hành, sử dụng bởi các Cơ quan quản lý dược chặt chẽ (SRA) như EMA, Nhật Bản, Anh, Úc, Canada, Thuỵ Sĩ… và tại các nước khu vực châu Á như: Nhật Bản, Hồng Kông, Maylasia, Thái Lan, Singapore, Đài Loan.
Cục Quản lý Dược cho biết, ngay sau khi nhận được thông tin nêu trên từ USFDA, Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc của Bộ Y tế đã tổ chức họp khẩn cấp vào ngày 31/1/2023 để xem xét về việc lưu hành, sử dụng thuốc Evusheld tại Việt Nam.
Trên cơ sở báo cáo, thông tin về các biến chủng của virus SARS-CoV-2 đang lưu hành tại Việt Nam, tình hình cấp phép, sử dụng Evusheld trên thế giới, cảnh báo của Tổ chức Y tế Thế giới (WHO) về đại dịch Covid-19 hiện vẫn là tình trạng khẩn cấp toàn cầu đối với sức khỏe cộng đồng,
Hội đồng kết luận thuốc Evusheld hiện vẫn có tác dụng đối với các biến chủng của virus SARS-Cov-2 đang lưu hành phổ biến tại Việt Nam.
Cục Quản lý Dược cũng thông tin, tại miền Bắc thông tin về tình hình giải trình tự gen các ca bệnh Covid-19 trên 541 mẫu thực hiện tại Viện Vệ sinh dịch tễ Trung ương, từ tháng 6 đến tháng 11, biến thể BA5 chiếm ưu thế, bên cạnh đó ghi nhận một số biến thể phụ khác như BA.2.74, BE.1.1; tháng 12, biến thể phụ BN.1.3 chiếm ưu thế; tiếp đó là các biến thể phụ BA.5.2, BA.2.75.6…
Ngoại trừ USFDA dừng cấp phép sử dụng do tình hình thực tiễn của các biến chủng SARS-CoV-2 lưu hành tại Hoa Kỳ, Evusheld hiện vẫn đang được cho phép lưu hành, sử dụng bởi các Cơ quan quản lý dược chặt chẽ (SRA) như EMA, Nhật Bản, Anh, Úc, Canada, Thuỵ Sĩ… và nhiều cơ quan quản lý dược trên thế giới.
Vì vậy, trên cơ sở phân tích tác dụng của thuốc với các biến chủng lưu hành tại Việt Nam và việc lưu hành, sử dụng thuốc tại các nước trên thế giới, Hội đồng thống nhất đề xuất tiếp tục cho phép lưu hành, sử dụng thuốc Evusheld tại Việt Nam.
Đồng thời, tiếp tục theo dõi, giám sát chặt chẽ và cập nhật thông tin về tính an toàn, hiệu quả của thuốc đối với các biến chủng của virus SARS-CoV-2 tại các nước trên thế giới và Việt Nam.

